TESTPAGINA ; niet geschikt / niet toegankelijk voor publiek gebruik
Hormoontherapie bij uitgezaaide borstkanker
Algemeen
Als u deze webpagina stap voor stap doorleest, begrijpt u veel beter waarom u deze behandeling krijgt aangeboden.
TIP: de informatie zeer uitgebreid dus neem uw tijd en lees de pagina in stukken.
Op deze webpagina wordt gesproken over de "palliatieve" behandeling. In deze situatie is de ziekte niet meer te genezen omdat er uitzaaiingen elders in het lichaam zijn vastgesteld. Bij de palliatieve behandeling is het doel van chemotherapie of andere medicamenteuze therapie (medicijnen) om de groei van de uitzaaiingen af te remmen en daarmee het leven te verlengen en behoud van kwaliteit van leven.
Nota bene: Het is belangrijk u te realiseren dat voor u persoonlijk de situatie anders kan zijn dan beschreven. Ook kunnen nieuwe resultaten voortkomend uit continu lopend wetenschappelijk onderzoek nog onderwerp zijn van discussie binnen de beroepsgroep. Hierdoor kan de visie omtrent de voordelen van de ene behandeling boven de andere behandeling op detail soms iets verschillen per behandelaar. Om toch tot een zoveel mogelijk uniforme behandeling in Nederland te komen, is een richtlijn opgesteld door een groot panel bestaande uit verschillende soorten oncologisch medisch specialisten (o.a chirurgen, internisten, radiotherapeuten e.a.). De richtlijn is te downloaden. Als er nieuwe inzichten zijn die door dit panel als zeer belangrijk worden ervaren, wordt de richtlijn aangepast. Door de snelle ontwikkelingen die momenteel plaatsvinden op het gebied van kankerbehandeling, is dit min of meer een continu proces.
Inleiding: Hoe werkt hormoontherapie bij uitgezaaide borstkanker
Bij hormoongevoelige (hormoonreceptor positief) tumoren wordt in eerste instantie begonnen met hormoontherapie tenzij er sprake is van snelle groei of grote uitzaaiingen in de organen. In die gevallen kan men er de voorkeur aan geven om direct met chemotherapie te starten. Hormoongevoelige tumoren komen vaker voor op hogere leeftijd: onder de 35 jaar ongeveer 50% en boven de 70 jaar ruim 80% (1).
Bij deze tumoren wordt celgroei gestimuleerd wanneer het vrouwelijke hormoon oestrogeen een verbinding maakt met de oestrogeenreceptoren op de kankercellen. Hormoontherapie is er op gebaseerd dat oestrogeen de oestrogeenreceptor niet meer kan stimuleren, waardoor de celgroei wordt geremd. Bij de keuze van de hormoontherapie is het belangrijk om een verschil te maken tussen vrouwen voor en na de overgang net zoals bij de adjuvante behandeling bij patiënten. (Zie behandeling met aanvullende (= adjuvante) hormoontherapie na de operatie waarbij als doel om uitzaaiingen te voorkomen.)
Bij meer dan de helft van de patiënten (50-70%) is er effect van de hormoontherapie: de uitzaaiingen worden niet groter en worden soms ook kleiner. Het duurt meestal enkele (drie) maanden voordat men resultaat ziet van deze medicijnen. Gemiddeld genomen is de duur van dit succes 12 tot 18 maanden, maar er zijn situaties waarbij er meerdere jaren een stabiele situatie optreedt en de uitzaaiingen niet groeien. Indien moet worden overgeschakeld naar een volgende lijn in de hormoontherapie neemt de succeskans echter af.
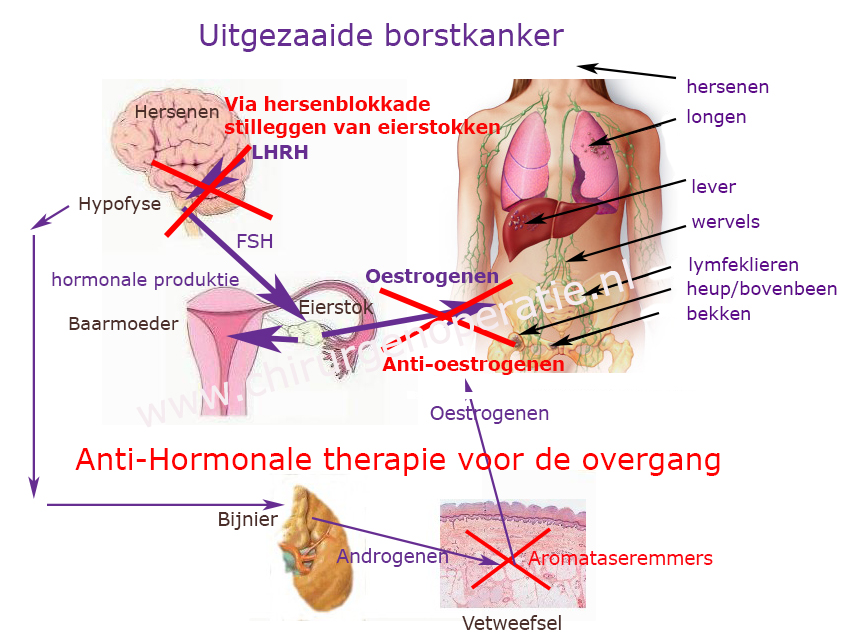
Hormoontherapie bij uitgezaaide borstkanker voor de overgang (zie figuur); de eierstokken produceren het vrouwelijk hormoon oestrogeen. Het hersenaanhangsel (hypofyse) regelt de productie van oestrogeen. Om de aanmaak van oestrogeen uit te schakelen, kunnen de eierstokken operatief worden verwijderd, maar kan ook de stimulatie door de hypofyse worden geblokkeerd. Via een andere route wordt in het vetweefsel ook een heel klein beetje oestrogeen gemaakt. Deze route speelt voor de overgang nauwelijks een rol aangezien de overgrote meerderheid oestrogeen wordt geproduceerd door de eierstokken.
Eerste lijn hormoontherapie: hoe werkt het
Bij een eerstelijnsbehandeling wordt meestal gebruik gemaakt van een combinatie waarbij;
- de productie van oestrogeen door de eierstokken wordt stilgelegd door toediening van periodieke injecties. Deze injecties heten leuproreline (Lucrin®) of gosereline (Zoladex®). Deze medicijnen worden LHRH-agonisten genoemd. Ze remmen de productie van FSH en LH in de hypofyse (hersenaanhangsel), waardoor de menstruele cyclus niet meer optreedt en het oestrogeengehalte daalt tot waarden vergelijkbaar met die na de overgang.
- Het effect van oestrogeen kan ook worden tegengewerkt door middel van tamoxifen dat de plaats van oestrogeen op de oestrogeenreceptor blokkeert. Dit medicijn is dus een anti-oestrogeen: het oestrogeen kan niet meer binden aan de oestrogeenreceptor op de borstkankercel. In geval van uitzaaiingen wordt tamoxifen meestal gecombineerd met het stilleggen van de oestrogeenproductie door de eierstokken.
Tweede lijn hormoontherapie: hoe werkt het
Als tweedelijnsbehandeling bij jonge patiënten kan een behandeling worden gegeven door het stilleggen van de oestrogeenproductie te combineren met een zogenoemde aromataseremmer.
Hormoontherapie bij uitgezaaide borstkanker na de overgang (zie figuur); de eierstokken produceren geen oestrogeen meer. Via een andere route wordt in het vetweefsel nog een heel klein beetje oestrogeen gemaakt. Deze aanmaak ontstaat op de volgende manier. In de bijnieren worden mannelijke (androgene) hormonen geproduceerd. Deze worden grotendeels in vetweefsel omgezet tot oestrogeen door het enzym “aromatase”. Aromataseremmers zijn medicijnen die dit enzym remmen en dus de productie van oestrogeen via het vetweefsel tegengaan.
Eerste lijn hormoontherapie: medicijnen
Met de eerste lijn hormoontherapie bij uitgezaaide borstkanker na de overgang worden deze aromataseremmers ingezet. De volgende aromataseremmers zijn beschikbaar: anastrozol (Arimidex®), exemestaan (Aromasin®) en letrozol (Femara®) (alfabetische volgorde).
Tweede / derde lijn hormoontherapie: medicijnen
De keuzes bij de tweede en derde lijn hormoontherapie zijn minder strak gedefinieerd en hebben met name als achterliggende gedachte om de hormooneffecten op iets andere wijze te bestrijden. In uw specifieke situatie zal uw medisch oncoloog samen met u beslissen welk medicijn het meest geschikt is of dat reeds moet worden overgeschakeld naar chemotherapie.
Het medicijn tamoxifen is een anti-oestrogeen. Het werkt het effect van oestrogeen tegen door de plaats van oestrogeen op de receptor te blokkeren door er zelf aan vast te koppelen. Zo wordt het oestrogeen de pas afgesneden. Fulvestrant (Faslodex®) is een medicijn, dat de werking van de receptor remt in de borstkankercellen en de receptor afbreekt.
| Schematisch overzicht hormoontherapie uitgezaaide borstkanker | ||
| Volgorde Medicijnkeuze | Voor de overgang | Na de overgang |
| 1e lijn | LHRH-agonist leuproreline of gosereline in combinatie met anti-oestrogeen tamoxifen |
Aromataseremmer |
| 2e lijn | LHRH-agonist leuproreline of gosereline in combinatie met aromataseremmer | Fulvestrant of tamoxifen |
| 3e lijn | Zie: na de overgang | Megestrolacetaat |
Doelgerichte therapie
Elk type doelgericht medicijn heeft zijn eigen doel (Engels: "target"): een schakel in een regelproces. Deze regelprocessen hebben invloed op de groei van een kankercel. Omdat het afweersysteem van de mens op vergelijkbare wijze ook heel doelgericht ten strijde trekt tegen bijvoorbeeld bacteriën wordt deze behandelmethode in de volksmond soms ook wel "immuuntherapie" genoemd. Doelgerichte medicijnen kunnen dus heel precies een regelproces ontregelen waardoor tumorgroei wordt stilgelegd.
Een kankercel kan zich wapenen tegen de remmende invloed van hormoontherapie en resistent worden. Dat laatste doet ze door via andere regelprocessen signalen binnen te halen die de cel stimuleren tot groei. Op deze wijze kan ze zich onttrekken aan de remmende invloed van hormoontherapie. De patiënt merkt dat doordat de uitzaaiing weer gaat groeien ondanks eerder succes met hormoontherapie. Doelgerichte therapie blokkeert op haar beurt deze ontsnappingsroutes waardoor hormoontherapie weer haar remmende invloed op de tumorcellen kan uitoefenen en de uitzaaiingen wederom tot groeistilstand komen en soms zelfs kleiner kunnen worden.
Er zijn verschillende soorten doelgerichte medicijnen:
- HER-2 remmers zoals trastuzumab (merknaam: Herceptin)
- M-TOR remmers zoals everolimus (merknaam: Afinitor)
- CDK4/6 remmers zoals abemaciclib (merknaam Verzenios), palbociclib (merknaam: Ibrance) en ribociclib (merknaam Kisquali)
HER-2 remmers: toevoegen aan hormoontherapie
Bij een klein aantal patiënten met een hormoongevoelige borstkanker is er ook sprake van HER2 overexpressie (lees meer …..). De toepassing van HER-2 remmers is de meest bekende doelgerichte therapie die ook al wordt gebruikt voor patiënten die geen uitzaaiingen hebben (zie elders op deze website).
Bij patiënten met uitgezaaide hormoongevoelige borstkanker waarbij bovendien HER2 overexpressie bestaat, is het mogelijk om trastuzumab of lapatinib toe te voegen aan een aromataseremmer. Er is aangetoond, dat de combinatie van een HER2-remmer en hormoontherapie verlenging geeft van de periode waarin de uitzaaiingen geen groei vertonen (groeistilstand) in vergelijking met hormoontherapie alleen. In vaktermen spreekt men over deze periode als de "progressievrije overlevingsperiode”". (kijk verder op de speciale pagina uitgezaaid HER2 positief.
M-TOR remmers: toevoegen van everolimus aan hormoontherapie
 Schematische weergave van groeisignaaloverdracht naar de celkern via het zogenaamde PI3K-AKT-mTOR regelproces. In de celwand, die is opgebouwd uit een dubbele laag vetzuren (1) bevinden zich diverse soorten receptoren die groeisignalen kunnen opvangen. Via deze receptoren wordt de groeisignaaloverdracht geactiveerd. Het eiwit mTOR (mammalian target of rapamycin) speelt een belangrijke rol in deze informatieoverdracht.(De PI3k, AKT en m-TOR eiwitten worden weergegeven op de figuur als blauwe zeshoeken)
Schematische weergave van groeisignaaloverdracht naar de celkern via het zogenaamde PI3K-AKT-mTOR regelproces. In de celwand, die is opgebouwd uit een dubbele laag vetzuren (1) bevinden zich diverse soorten receptoren die groeisignalen kunnen opvangen. Via deze receptoren wordt de groeisignaaloverdracht geactiveerd. Het eiwit mTOR (mammalian target of rapamycin) speelt een belangrijke rol in deze informatieoverdracht.(De PI3k, AKT en m-TOR eiwitten worden weergegeven op de figuur als blauwe zeshoeken)
Bij patiënten met een hormoongevoelige borstkanker is hormoontherapie na verloop van tijd niet meer effectief. Men spreekt dan van resistentie. De borstkankercel kan weer gaan groeien, omdat deze groeisignalen opvangt door activering van andere informatieroutes. Één van die routes is de PI3K-AKT-mTOR route. (zie figuur). Speciale doelgerichte medicijnen die kunnen doordringen in de borstkankercel en dit eiwit kunnen blokkeren worden “mTOR-remmers” genoemd.
Door patiënten bij wie de ziekte weer actief is en die eerder letrozol of anastrozol kregen de mTOR remmer, everolimus (Afinitor®), voor te schrijven in combinatie met exemestaan kan de ziekte soms enkele maanden langer onder controle worden gehouden (= verlenging van de progressievrije overleving). Dit is in de zogenoemde BOLERO-2 studie aangetoond. Door vrouwen met een HER2-negatieve, hormoongevoelige borstkanker die eerder anastrozol of letrozol kregen over te zetten op exemestaan in combinatie met everolimus werd de ziekte gemiddeld ruim 11 in plaats van 4 maanden langer onder controle gehouden. Op deze wijze kan het tijdstip van starten met chemotherapie met een half jaar worden uitgesteld (2).
Het gebruik van everolimus leidt wel tot bijwerkingen, Uw medisch oncoloog zal samen met u uitzoeken of het medicijn nuttig kan zijn in uw situatie met zoveel mogelijk behoud van kwaliteit van leven.
CDK4/6-remmers: Toevoegen van CDK4/6-remmers aan hormoontherapie
Het regelproces voor celgroei heeft veel verschillende schakels die het doel kunnen zijn van doelgerichte therapie. Twee belangrijke schakels in dit proces zijn de eiwitten CDK4 en CDK6. Palbociclib en ribociclib zijn nieuwe medicijnen, die deze eiwitten selectief remmen in activiteit. Celgroei wordt hierdoor stilgelegd.
Achtergrond informatie
De cyclus waarbij een cel zich deelt in 2 nieuwe identieke cellen loopt volgens een vast patroon waarbij verschillende fasen worden doorlopen.
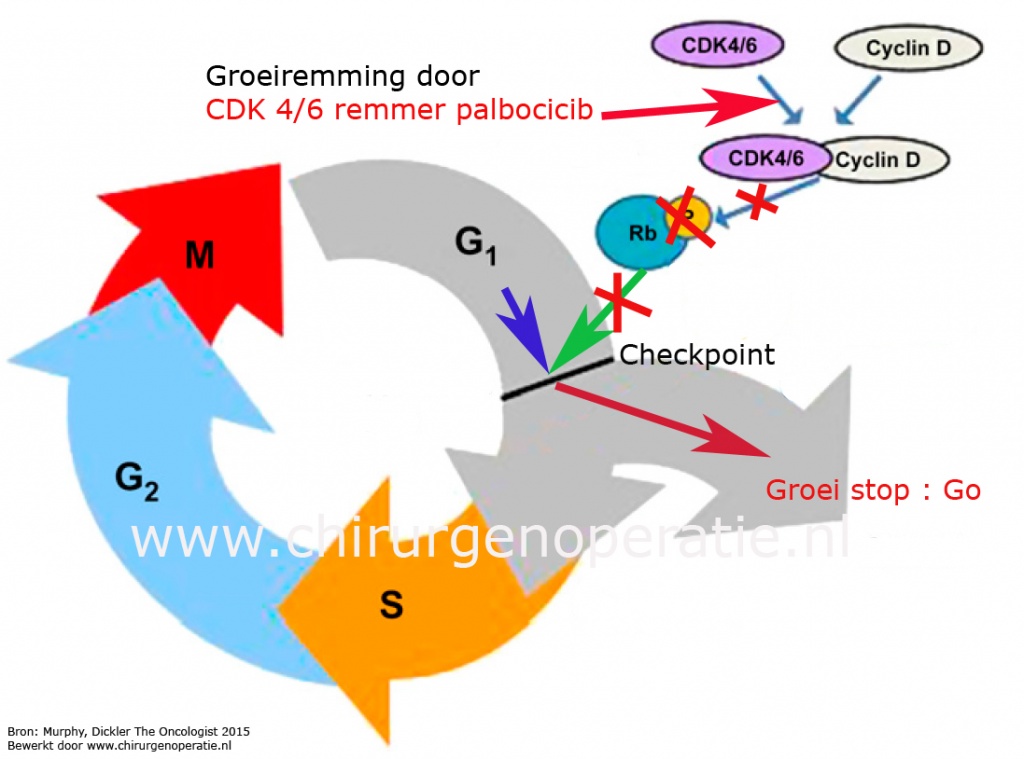
Op bijgaande figuur zijn deze fasen uitgelegd.
Een cel die zich actief deelt, bijvoorbeeld de borstkankercel, verzamelt in de G1-fase (G staat voor "gap") voldoende bouwstoffen en energiereserves om uit te groeien tot een volwassen cel en zich vervolgens voor te bereiden op een nieuwe celdeling.
Indien de cel niet tot verdere groei wordt gestimuleerd valt ze in een soort "rust-fase": Go.
Cellen in de Go-kunnen zich verder specialiseren waarbij als voorbeeld de zenuwcellen in de hersenen. Andere voorbeelden zijn cellen die samen de lever vormen: ze verkeren in de Go-fase maar kunnen als het moet weer terugkeren in de G1 fase om vervolgens te delen. Op deze wijze kan een lever gedeeltelijk aangroeien nadat een deel is verwijderd.
Cellen die niet meer in de G1 fase terugkeren – en dus stilvallen – verouderen en in geval van kanker zal het gezwel niet verder groeien, tot stilstand komen en uiteindelijk afsterven door ouderdom.
Om verder te gaan (blauwe pijl) naar de S-fase moet de cel eerst een zogenaamd checkpoint passeren. Onder invloed van een stimulerende impuls (groene pijl) van een schakeling van diverse enzymen/eiwitten – waaronder een eiwitcomplex bestaande uit cycline (grijze ovaal) en CDK4/CDK6 (paarse ovaal) – wordt een cel als het ware de S-fase in "geduwd".
Eenmaal in de S-fase wordt het cel-DNA gekopieerd tot 2 identieke sets.
In de aansluitende G-2 fase bereidt de cel zich voor op de daadwerkelijke deling die plaatsvindt tijdens de M-fase: mitose. Hier wordt het DNA verdeeld in 2 identieke sets chromosomen. Vervolgens splitst de cel zich in 2 identieke cellen met gelijke hoeveelheid DNA en andere bestanddelen.
CDK4/6-remmers grijpen heel specifiek aan bij de CDK4 en CDK6 eiwitten (rode pijl). Hierdoor kan er geen binding met het cycline eiwit worden gemaakt en dus geen stimulerende activiteit op de cel in de G1 fase (rode kruisen). De kankercel valt in een rustfase (Go). De groeit van het gezwel komt tot stilstand. Uit experimentele studies is gebleken dat CDK4/6-remmers het beste werken in hormoongevoelige borstkanker.
Klinische studieresultaten met toevoeging van CDK4/6 remmers
Sinds 2014 zijn er resultaten bekend gemaakt van verschillende klinische studies met CDK4/6-remmers bij patiënten met hormoongevoelige uitgezaaide borstkanker waarbij deze middelen al of niet waren toegevoegd aan de bestaande antihormoontherapie met letrozol. Hierbij werd aangetoond dat de periode waarbij de ziekte tot stilstand (Go-fase) kon worden gebracht ("progressievrije overlevingsperiode”") werd verlengd van ruim 10 maanden (alleen letrozol) naar ruim 2 jaar. Alhoewel de ziekte langer tot stilstand kon worden gebracht werd is het nog niet duidelijk of patiënten die deze middelen gebruiken aan het begin van hun behandeling voor uitgezaaide hormoongevoelige borstkanker langer overleven dan patiënten waarbij deze middelen niet worden ingezet. Toch kan een dergelijke verlenging uitermate zinvol zijn en bijdragen aan de kwaliteit van leven.
Bijwerkingen vaak gezien bij cdk4/6-remmers zijn met name een afname van de afweer (infecties) en afname van het aantal witte bloedcellen, rode bloedcellen en bloedplaatjes. Daarnaast ook een wisselende mate van moeheid, diarree en misselijkheid.
Inmiddels lopen en meerdere studies waarbij palbociclib of ribociclib vanaf het het eerste moment dat uitgezaaide borstkanker wordt vastgesteld aan letrozol worden toegevoegd (PALOMA-2 & MONALEESA-2 studies). De PALOMA-3 studie met palbociclib is vergelijkbaar maar daarbij wordt fulvestrant als antihormonale therapie gebruikt.
Om uit te vinden op welk moment een CDK4/6-remmer het beste past in de behandeling heeft de Nederlandse Borstkanker Onderzoeksgroep (BOOG) de SONIA studie. opgezet. In dit onderzoek wordt onderzocht op welk moment van de loop van de behandeling de CDK4/6-remmers (palbociclib of ribociclib) het beste aan de anti-hormonale therapie kunnen worden toegevoegd op het moment dat uitzaaiingen worden vastgesteld. Om te zien welke behandelingsvolgorde (direct of pas later) beter is, moeten de twee behandelingen met elkaar worden vergeleken. Om dat te kunnen doen, worden de deelnemers aan het onderzoek in twee groepen verdeeld. De ene groep zal direct (1e lijn) starten met anti-hormonale therapie (een aromataseremmer) EN een CDK4/6-remmer en bij ziektetoename (progressie) alleen de anti-hormonale therapie fulvestrant (2e lijn). De andere groep start in het begin (1e lijn) alleen een aromataseremmer en pas bij onvoldoende resultaat wordt de CDK4/6 remmer toegevoegd (2e lijn): de combinatie fulvestrant + CDK4/6-remmer.
In MONARCH 2-studie, waarbij abemaciclib plus fulvestrant werd vergeleken met fulvestrant plus een placebo (= schijnmedicijn), werd onlangs op het ESMO congres 2019 gemeld dat bij vrouwen met een hormoongevoelig uitgezaaide borstkanker niet alleen de ziekte effectief voor langere tijd (meer dan 6 maanden) kon worden stilgelegd maar ook dat vrouwen langer in leven bleven: van gemiddeld 37 naar 46 maanden. Met name het langer uitstellen van de noodzaak om toch te moeten overschakelen naar chemotherapie (van 22 naar 50 maanden) is voor de dagelijkse praktijk een belangrijke bevinding.
Ook bij HER2+ uitgezaaide borstkanker blijkt toevoeging van de CDK4/6 remmer ademaciclib naast trastuzumab als doelgerichte therapie de ziekte enkele maanden extra langer stil te kunnen leggen (MonarcHER studie).
Bronvermelding:
- Bentzon N et al. Prognostic effect of estrogen receptor status across age in primary breast cancer. Int J Cancer 2008;122:1089-1094.
- BOLERO-2 studie: Baselga J, Campone M, et al. Everolimus in postmenopausal hormone-receptor-positive advanced breast cancer. N Engl J Med. 2012 Feb 9;366(6):520-9.
- PALOMA-2 studie: Finn et al. Palbociclib and Letrozole in Advanced Breast Cancer N Engl J Med 2016;375:1925-36.
- Hortobagyi GN et al, Ribociclib as First-Line Therapy for HR-Positive, Advanced Breast Cancer. N Engl J Med. 2016 Nov 3;375(18):1738-1748.
- Cristofanilli et al. Fulvestrant plus palbociclib versus fulvestrant plus placebo for treatment of hormone-receptor-positive, HER2-negative metastatic breast cancer that progressed on previous endocrine therapy (PALOMA-3): fi nal analysis of the multicentre, double-blind, phase 3 randomised controlled trial. Lancet Oncol 2016; 17: 425–39.
- SONIA studie
- Sledge et al. The Effect of Abemaciclib Plus Fulvestrant on Overall Survival in Hormone Receptor-Positive, ERBB2-Negative Breast Cancer That Progressed on Endocrine Therapy-MONARCH 2: A Randomized Clinical Trial. JAMA Oncol 2019 Sep 29
Surgipoort dankt mw. prof. dr. E. Boven, internist oncoloog van VUmc Cancer Center Amsterdam, voor het redactioneel commentaar en aanvullingen bij het opstellen van deze webpagina (excl. onderdeel CDK4/6 remmers)